Le diabète de type 2 dévoilé : Un guide pour les étudiants en médecine
Par Dr. Miriam Sonntag
La Fédération internationale du diabète (FID) tire la sonnette d'alarme avec une statistique stupéfiante : 537 millions de personnes dans le monde vivaient avec le diabète rien qu'en 2021. Cela représente 1 adulte sur 10, et les chiffres devraient monter en flèche (1). Dans cet article de blog, nous allons percer les secrets du diabète de type 2, le champion en titre du diabète, qui représente jusqu'à 90 % des cas diagnostiqués (1). Nous dévoilerons la résistance à l'insuline et vous fournirons les outils nécessaires pour combattre et prévenir cette épidémie galopante.
Homéostasie du glucose
Avant de plonger dans la résistance à l'insuline, passons d'abord en revue les conditions normales. Le glucose alimente nos tissus, mais le maintien de l'équilibre est vital. L'homéostasie du glucose nécessite la coordination de plusieurs organes et tissus. Les organes clés de coordination sont le pancréas, le foie, les muscles et le tissu adipeux.
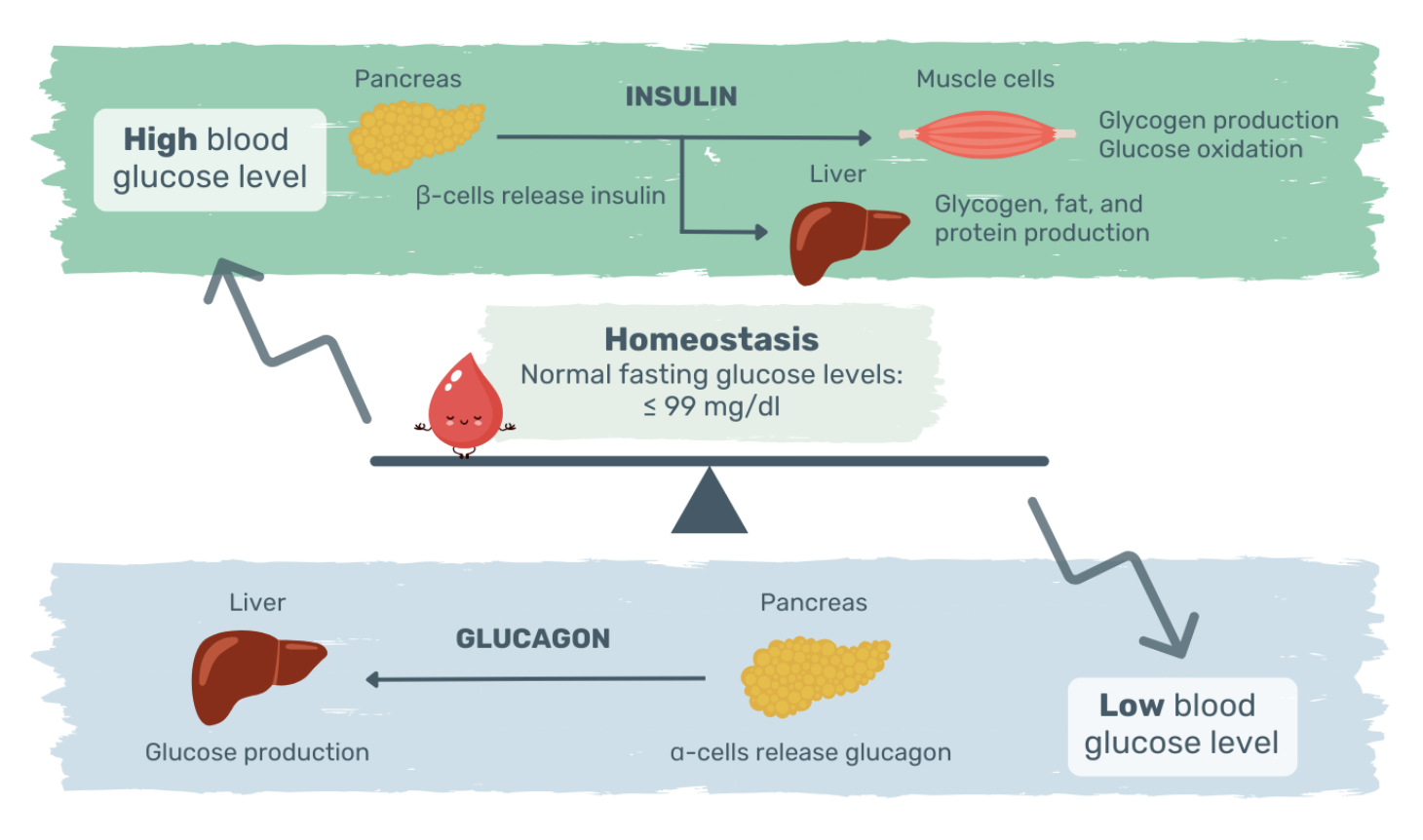
Le pancréas détecte les fluctuations de la glycémie et y répond. Il assure l'homéostasie du glucose en sécrétant du glucagon et de l'insuline, deux hormones opposées. Lorsque la glycémie est faible, les cellules ɑ du pancréas libèrent du glucagon. Le glucagon stimule la production hépatique de glucose.
En revanche, lorsque la glycémie est élevée, les cellules β du pancréas sécrètent l'hormone anabolisante qu'est l'insuline. Le glucose pénètre dans les cellules β par les transporteurs GLUT2, où il est phosphorylé par la glucokinase. Cette enzyme de détection du glucose adapte la production d'insuline au glucose circulant (2).
L'insuline favorise l'absorption du glucose dans les cellules musculaires et adipeuses. L'insuline se lie au récepteur de l'insuline sur la membrane plasmique de la cellule cible (3). Elle déclenche la translocation des vésicules du transporteur GLUT4 vers la membrane plasmique. Une fois inséré dans la membrane plasmique, le transporteur GLUT4 permet au glucose de pénétrer dans la cellule. Les cellules musculaires ont une grande capacité de stockage du glucose, représentant jusqu'à 70 % de l'élimination du glucose après les repas (4,5).
L'insuline abaisse la glycémie non seulement en favorisant l'élimination du glucose dans les tissus cibles. Dans le foie, l'insuline supprime la production hépatique de glucose et stimule la synthèse des protéines, des lipides et du glycogène. À l'état basal, il faut très peu d'insuline pour supprimer la production hépatique de glucose.
Résistance à l'insuline
Le diabète de type 2 est une maladie progressive. La sécrétion d'insuline diminue et son efficacité s'amenuise. Les cellules cibles deviennent résistantes à l'insuline. Au stade précoce, connu sous le nom de prédiabète, le pancréas compense la baisse de l'efficacité de l'insuline en produisant davantage d'insuline. Cependant, avec le temps, le pancréas commence à s'user et la capacité de sécrétion d'insuline diminue. Cette baisse constante de la fonction des cellules bêta diminue la sensibilité au glucose. Lorsque le diagnostic de diabète de type 2 est posé, le nombre de cellules bêta fonctionnelles est inférieur à 50 % (6).
Le diabète de type 2 augmente le risque d'athérosclérose, de neuropathie et de syndrome du pied diabétique, ainsi que de néphropathie et de rétinopathie, l'une des principales causes de cécité due à la déficience visuelle (1). Cependant, le diabète peut être complètement inversé avec une bonne approche et une intervention précoce. Voyons cela de plus près.
Cause fondamentale de la résistance à l'insuline
Des études suggèrent que la résistance à l'insuline est causée par un excès de graisse abdominale et ectopique. L'excès de graisse abdominale est également connu sous le nom d'obésité centrale. Il est en corrélation avec le tour de taille. Plus le tour de taille est important, plus le risque de diabète est élevé (7).
Le tissu adipeux est le seul tissu conçu pour tolérer des niveaux élevés d'acides gras. Pourtant, sa capacité est limitée. Lorsque cette capacité est dépassée, l'excès d'énergie déclenche une inflammation du tissu adipeux, ce qui entraîne une altération de la signalisation de l'insuline et une augmentation des acides gras libres en circulation.
Ces acides gras libres en circulation peuvent alors infiltrer le foie, les muscles et le pancréas, formant des réserves de graisse ectopiques. L'accumulation de graisse dans le muscle empêche l'entrée du glucose dans la cellule. Les vésicules du transporteur GLUT4 ne sont pas transloquées vers la membrane cellulaire.
De même, lorsque la graisse s'accumule dans le foie, l'insuline devient moins efficace pour empêcher la production hépatique de glucose. De plus, l'infiltration d'acides gras libres dans le pancréas augmente l'inflammation, le dysfonctionnement mitochondrial et l'apoptose. Cela conduit à la fibrose du pancréas et à la mort des cellules β. Par conséquent, la capacité de sécrétion d'insuline diminue tandis que les niveaux de glucose dans le plasma restent élevés.
Le diabète de type 2 est une maladie complexe qui peut mettre des années, voire des décennies, à se manifester. Un poids corporel insuffisant contribuant à 80-85 % du risque, il s'agit avant tout d'une affection liée au mode de vie (8). Toutefois, l'adoption d'un mode de vie favorisant un poids corporel sain peut prévenir ou inverser le diabète de type 2.
La nutrition comme solution
Il existe des preuves solides que la perte de poids peut retarder la progression de la résistance à l'insuline vers le diabète. Chez les patients obèses, une perte de poids de 5 à 10 % permet non seulement d'améliorer le contrôle de la glycémie, mais aussi de réduire les besoins en médicaments. En outre, une perte de poids substantielle peut abaisser le taux d'HbA1c et mettre le diabète en rémission (9).
L'étude DiRECT sur le diabète a comparé le traitement standard du diabète à la restriction calorique pour la perte de poids. Après 12 mois, les taux de rémission étaient de 46 % dans le groupe d'intervention et de seulement 4 % dans le groupe de contrôle. Cette étude souligne que la rémission dépend de la perte de poids. Dans le groupe d'intervention, 86 % des patients ayant perdu plus de 15 kg ont obtenu une rémission. Dans le groupe de contrôle, aucun patient ayant pris du poids n'a obtenu de rémission (10).
Si la perte de poids est essentielle pour vaincre le diabète de type 2, comment y parvenir ? Il est possible de perdre du poids en suivant n'importe quel régime, même un régime à base de malbouffe ultra-transformée. Mais il est peu probable que l'on puisse suivre un tel régime à long terme tout en se sentant bien.
Des études suggèrent que la qualité de l'alimentation joue un rôle crucial dans la prévention ou l'inversion du diabète. La consommation d'un excès de calories, de graisses saturées, de cholestérol, de viande rouge et de sucre ajouté amplifie le risque de diabète (11). À l'inverse, l'incorporation d'aliments végétaux entiers peut réduire le risque de diabète (11).
Dans l'étude EPIC (European Prospective Investigation into Cancer and Nutrition) menée auprès de plus de 38 000 participants, les chercheurs ont conclu que chaque tranche de 5 % de calories provenant de protéines, en particulier de protéines animales, entraînait une augmentation de 30 % du risque de développer un diabète de type 2. Aucune association de ce type n'a été trouvée pour les protéines d'origine végétale (12).
En outre, dans une étude comparant un régime végétalien pauvre en graisses aux soins standard de l'American Diabetes Association, le groupe végétalien a obtenu des résultats remarquables : Ils ont divisé par deux leur consommation de médicaments (48 % contre 23 %), réduit trois fois plus leur taux d'HbA1c (-1,23 % contre -0,38 %), perdu deux fois plus de poids (6,5 kg contre 3 kg) et réduit deux fois plus leur taux de cholestérol LDL (21,2 % contre 9,3 %) (13).
Les régimes alimentaires à base de plantes peuvent prévenir et traiter le diabète. Cependant, tous les aliments d'origine végétale ne sont pas bons pour la santé. Les données de trois études de cohortes américaines, qui ont suivi plus de 200 000 professionnels de la santé pendant plus de 20 ans, ont mis en évidence l'impact des décisions en matière d'alimentation. Les régimes privilégiant les aliments végétaux entiers ont vu leur risque de diabète diminuer de 34 %. En revanche, les régimes à base de plantes riches en aliments transformés présentaient un risque de diabète accru de 16 % (14).
Les végétaux non transformés sont riches en fibres, qui alimentent les bactéries intestinales. Si vos microbes sont bien nourris, ils produisent une multitude de métabolites bénéfiques. Les acides gras à chaîne courte, comme le butyrate, peuvent améliorer la clairance du glucose dans le sang (15).
En revanche, les aliments transformés doivent être limités ou évités. Remplacer les graisses saturées par des graisses polyinsaturées ou des glucides non raffinés, par exemple, peut améliorer la sensibilité à l'insuline (16). En outre, plus nous consommons d'aliments transformés, plus le risque de diabète est élevé (17).
Message à retenir
Les aliments végétaux complets réduisent non seulement le risque de développer un diabète de type 2, mais ils peuvent également rétablir une physiologie normale chez les patients souffrant d'une résistance à l'insuline ou d'un diabète de type 2. En outre, les aliments végétaux ont une densité calorique inférieure à celle des aliments ultra-transformés et des aliments d'origine animale. Ils peuvent contribuer à créer un déficit calorique et à favoriser un poids corporel sain.
Prêt à faire découvrir à vos patients les bienfaits d'un régime à base d'aliments complets et de plantes ? Explorez nos conseils ci-dessous ou découvrez nos cartes Change Talk. Elles sont conçues pour aider vos patients à surmonter toute objection à un changement positif.
Conseils pour encourager vos patients à manger sainement
Concentrez-vous sur les aliments que vous ajoutez, et non sur ceux que vous supprimez.
Commencez par les aliments végétaux que vous connaissez et appréciez déjà, puis élargissez votre liste.
Planifiez vos plats préférés : remplacez les ingrédients malsains par des alternatives végétales nourrissantes.
Mangez l'arc-en-ciel : Essayez de consommer 30 plantes différentes par semaine.
Gardez des fruits frais à portée de main : C'est un en-cas parfait et sain pour satisfaire les envies de sucré.
Rebondir : accepter les rechutes, se réinitialiser et reprendre une alimentation saine.
Informations complémentaires :
-
Dr Miriam Sonntag is the Medical Content Executive of the online learning platform, PAN Academy. Having worked in basic research, she knows how to decipher complex information. Working now at PAN, she scans and pours over scientific papers and books. She breaks down the latest nutritional research into actionable advice for everyday life. She is committed to sharing the bigger picture of why it is good to put more plants on your plate.
-
International Diabetes Federation, 2021. IDF Diabetes Atlas 2021. Available from: https://diabetesatlas.org/atlas/tenth-edition/
Bae et al., 2010. Transcriptional Regulation of Glucose Sensors in Pancreatic β-Cells and Liver: An Update. Available from: https://doi.org/10.3390%2Fs100505031
Petersen & Shulman, 2018. Mechanisms of Insulin Action and Insulin Resistance. Available from: https://doi.org/10.1152%2Fphysrev.00063.2017
Jensen et al., 2011. The Role of Skeletal Muscle Glycogen Breakdown for Regulation of Insulin Sensitivity by Exercise. Available from: https://doi.org/10.3389%2Ffphys.2011.00112
Chadt & Al-Hasani, 2020: Glucose transporters in adipose tissue, liver, and skeletal muscle in metabolic health and disease. Available from: https://doi.org/10.1007/s00424-020-02417-x
Taylor, 2013. Banting Memorial lecture 2012: reversing the twin cycles of type 2 diabetes. Available from: https://doi.org/10.1111/dme.12039
Jayedi et al., 2022. Anthropometric and adiposity indicators and risk of type 2 diabetes: systematic review and dose-response meta-analysis of cohort studies. Available from: https://doi.org/10.1136/bmj-2021-067516
Shah, 2015. Assessing the risk of diabetes. Available from: https://doi.org/10.1136/bmj.h4525
ElSayed et al., 2022. 8. Obesity and Weight Management for the Prevention and Treatment of Type 2 Diabetes: Standards of Care in Diabetes—2023. Available from: https://doi.org/10.2337/dc23-Sint
Lean et al., 2018. Primary care-led weight management for remission of type 2 diabetes (DiRECT): an open-label, cluster-randomised trial. Available from: https://doi.org/10.1016/S0140-6736(17)33102-1
Kolb & Martin, 2017. Environmental/lifestyle factors in the pathogenesis and prevention of type 2 diabetes. Available from: https://doi.org/10.1186/s12916-017-0901-x
Sluijs et al., 2009. Dietary Intake of Total, Animal, and Vegetable Protein and Risk of Type 2 Diabetes in the European Prospective Investigation into Cancer and Nutrition (EPIC)-NL Study. Available from: https://doi.org/10.2337/dc09-1321
Barnard et al., 2006. A Low-Fat Vegan Diet Improves Glycemic Control and Cardiovascular Risk Factors in a Randomized Clinical Trial in Individuals With Type 2 Diabetes. Available from: https://doi.org/10.2337/dc06-0606
Satija et al., 2016. Plant-Based Dietary Patterns and Incidence of Type 2 Diabetes in US Men and Women: Results from Three Prospective Cohort Studies. Available from: https://doi.org/10.1371%2Fjournal.pmed.1002039
Salamone et al., 2021. The relationship between gut microbiota, short-chain fatty acids and type 2 diabetes mellitus: the possible role of dietary fibre. Available from: https://doi.org/10.1007/s00592-021-01727-5
Luukkonen et al., 2018. Saturated Fat Is More Metabolically Harmful for the Human Liver Than Unsaturated Fat or Simple Sugars. Available from: https://doi.org/10.2337/dc18-0071
Moradi et al., 2021. Ultra-Processed Food Consumption and Adult Diabetes Risk: A Systematic Review and Dose-Response Meta-Analysis. Available from: https://doi.org/10.3390%2Fnu13124410